
当血细胞学会“P图”——以一例假性高钾血症去伪求真
作者:覃维,黄一芳,广西医科大学,广西医科大学第一附属医院检验科
前言
高钾血症 (Hyperkalemia)是临床常见的电解质紊乱,严重时可引发致命性心律失常
(Hyperkalemia)是临床常见的电解质紊乱,严重时可引发致命性心律失常 。准确识别其真伪,是保障患者安全的关键环节。
。准确识别其真伪,是保障患者安全的关键环节。
假性高钾血症(Pseudohyperkalemia)特指体外因素导致的血清钾浓度假性升高,而患者体内真实血钾水平正常的一种实验室现象[1]。这一现象的漏判或误判,极易引发临床过度治疗,可能导致医源性低钾血症 、不必要的心脏监护甚至药物不良反应,增加医疗风险与资源消耗。
、不必要的心脏监护甚至药物不良反应,增加医疗风险与资源消耗。
对于伴有显著血小板、白细胞及/或红细胞增多的患者,其假性高钾血症的发生风险显著增高,机制涉及凝血过程中血小板活化释钾、白细胞代谢耗竭致钾泵失能以及大量红细胞作为钾储备库的体外影响。
因此,建立对此现象的系统认知、保持高度警惕,并掌握规范有效的鉴别流程,对于检验科而言,是确保报告准确性、辅助临床精准决策的核心职责;对于临床而言,则是避免误诊误治、保障患者安全的重要防线。
案例经过
1、主要病史
患者:女,40岁。主诉:颜面、双手皮肤潮红1年,伴间断头晕、乏力。
诊疗经过:患者因上述症状曾于外院就诊,行冠脉造影、头颅CT等检查未见明确器质性病变,予氯吡格雷 、阿托伐他汀
、阿托伐他汀 治疗后肢体麻木等症状有所缓解,但皮肤潮红及头晕主症持续。为进一步明确病因,门诊以“红细胞增多”收入血液科。
治疗后肢体麻木等症状有所缓解,但皮肤潮红及头晕主症持续。为进一步明确病因,门诊以“红细胞增多”收入血液科。
初步印象:临床表现集中于皮肤血管与神经系统,病史较长且相对平稳,诊断方向指向血液系统疾病可能。
2、入院检查
为评估病情,患者入院后即完善常规实验室检查。部分结果如下:
2.1 血生化:
①血清钾:6.20 mmol/L(参考范围 3.5-5.3 mmol/L)(见图1),显著高于危急值阈值。
②其他指标:肾功能、其余电解质等基本正常(见图1、图2)。
2.2血常规 :结果显示白细胞、红细胞、血小板均显著增多(见图3),符合“外周血全血细胞增多”的实验室特征。
:结果显示白细胞、红细胞、血小板均显著增多(见图3),符合“外周血全血细胞增多”的实验室特征。
3、初步排查与应急处理
面对高危检验结果与平稳临床表现的矛盾,检验科立即启动复核查验程序:
①复核标本与质控:确认标本无溶血、脂血、凝块,当日质控在控,仪器无偶然误差。(见图4、图5)
②临床路径溯源:确认患者无静脉补钾史,未使用显著影响血钾的药物;无高钾血症典型的肌无力、心律失常等临床表现,心电图 亦无相应改变,仅为窦性心律。(见图6)
亦无相应改变,仅为窦性心律。(见图6)
如此孤立且严重的高钾血症,其真实性存疑。
③关联数据分析:肾功能、其余电解质等基本正常,结合显著增高的全血细胞计数 ,高度怀疑为“假性高钾血症”。
,高度怀疑为“假性高钾血症”。
④紧急沟通与规范复查:立即按危急值流程通知临床,建议并指导使用肝素 锂抗凝管(Lithium Heparin Tubes)重新采集静脉血,以检测不受体外凝血过程干扰的血浆钾水平。
锂抗凝管(Lithium Heparin Tubes)重新采集静脉血,以检测不受体外凝血过程干扰的血浆钾水平。
4、复查结果与最终判定
重新采血后,肝素锂抗凝管检测结果显示:血浆钾4.75 mmol/L,完全处于正常参考区间内。(见图7)
该结果与促凝管血清钾结果存在巨大差异,确证了此前的高钾为体外因素导致的假性升高。审核并发布准确报告,同时在报告中备注了可能的原因,避免临床误判与不必要干预。至此,一例假性高钾血症得以成功识别与纠正。
案例分析
1、锁定矛盾
患者因“皮肤潮红”入院,无高钾血症相关临床表现(如肌无力、心律失常),心电图也无相应改变。然而,促凝管(Serum Separating Tubes , SST)检测的血清钾高达6.20 mmol/L,达到危急值水平。这种检验与临床的显著矛盾,急需检验人鉴别“真假高钾”。
2、关联线索
面对矛盾,首要步骤是核查关联信息。查阅患者血常规结果,发现白细胞、红细胞及血小板均显著增多,符合“外周血全血细胞增多”,为解释血清钾假性升高提供了直接、合理的嫌疑指向。血细胞释放钾离子的风险极高。
3、机制剖析
在“多细胞增多”背景下,SST成为体外干扰的主因。
假性高钾的机制为多因素协同:
①血小板活化是主因(胞内钾浓度约为血浆30倍[1]),促凝剂触发其聚集释钾;
②白细胞增多加速体外三磷酸腺苷 (Adenosine Triphosphate, ATP)耗竭,致使 Na⁺/K⁺-ATP酶(钠钾泵, Sodium-Potassium-Exchanging ATPase)功能衰竭[1-2]。胞内钾外流,加剧钾累积。
(Adenosine Triphosphate, ATP)耗竭,致使 Na⁺/K⁺-ATP酶(钠钾泵, Sodium-Potassium-Exchanging ATPase)功能衰竭[1-2]。胞内钾外流,加剧钾累积。
③红细胞作为最大钾库(胞内钾浓度约为血浆25倍)[1],在高细胞压积下易受离心机械损伤而释钾。
④采血至离心的延迟及离心力破坏细胞团块,进一步放大钾释放幅度。
4、方法验证
要获得真实反映体内循环的血钾水平,必须阻断凝血过程、保持细胞稳定、缩短体外时间。肝素锂抗凝管正是为此设计:通过抗凝作用阻止血小板活化,保持红细胞和白细胞的膜稳定性;维持血液液态以快速分离血浆,减少细胞体外代谢时间。
本例更换肝素管后测得的血浆钾为4.75 mmol/L,结果正常。与血清钾的显著差异,确证高钾为体外假象。
综上,本例考虑为“外周血全血细胞增多导致的假性高钾血症”。诚然,在遇到高钾血症时,若同时伴有任何一系或多系血细胞显著增多,均应高度怀疑假性高钾的可能。
知识拓展
除外周血全血细胞增多外,以下因素同样值得考虑:
1、溶血(体外溶血)
机制:红细胞内钾浓度约为血浆25倍,红细胞破裂直接释放大量钾离子。
识别关键:通常伴有乳酸脱氢酶(L-Lactate Dehydrogenase, LDH)、游离血红蛋白 (Free Hemoglobin)的同步异常升高,血清/血浆呈粉红色或红色,轻度溶血需依赖溶血指数(Hemolysis Index)客观判断。
(Free Hemoglobin)的同步异常升高,血清/血浆呈粉红色或红色,轻度溶血需依赖溶血指数(Hemolysis Index)客观判断。
2、采血技术不规范
①止血带使用过久或反复握拳:局部组织缺血、酸中毒,促使细胞内钾外移。止血带使用>1分钟,可使血钾升高0.2 mmol/L以上[1]。
②采血针过细或抽吸力过大:造成机械性溶血。
3、标本处理与运输不当
①温度异常:高温(>25℃)加速细胞代谢耗尽ATP;低温(4℃或冰上)抑制钠钾泵,可能诱导遗传性疾病红细胞钾泄漏[1]。
②延迟分离:细胞体外持续糖酵解消耗ATP,导致钾外流。
③剧烈震荡运输:对白细胞极高或存在病态脆性细胞的标本,易致细胞破裂。
4、标本污染
①乙二胺四乙酸(Ethylenediaminetetraacetic acid , EDTA)污染:最常见且危险。血液回流或采血顺序错误致EDTA-K₂污染生化管,钾假性显著升高,钙被螯合而假性降低。
②含钾消毒剂污染。
③静脉输液侧采血。
5、罕见遗传性与特殊疾病
①家族性假性高钾血症(Familial Pseudohyperkalemia):常染色体 显性遗传,因红细胞膜蛋白相关基因突变,如压电型机械敏感离子通道组件1(piezo-type mechanosensitive ion channel component 1, PIEZO1)和ATP结合盒亚家族G成员6(ATP-binding cassette subfamily G member 6,ABCG6) ,导致红细胞在低温下钾异常外漏[1]。
显性遗传,因红细胞膜蛋白相关基因突变,如压电型机械敏感离子通道组件1(piezo-type mechanosensitive ion channel component 1, PIEZO1)和ATP结合盒亚家族G成员6(ATP-binding cassette subfamily G member 6,ABCG6) ,导致红细胞在低温下钾异常外漏[1]。
②反向假性高钾血症(Reverse Pseudohyperkalemia):见于慢性淋巴细胞白血病 (Chronic Lymphocytic Leukemia, CLL)或肿瘤溶解综合征(Tumor Lysis Syndrome, TLS),肝素可能诱导脆性淋巴细胞体外破裂,此时动脉血气分析
(Chronic Lymphocytic Leukemia, CLL)或肿瘤溶解综合征(Tumor Lysis Syndrome, TLS),肝素可能诱导脆性淋巴细胞体外破裂,此时动脉血气分析 (Blood Gas Analysis)是更可靠金标准。
(Blood Gas Analysis)是更可靠金标准。
怀疑假性高钾时,以下方法有助于获取可靠结果(见表1):
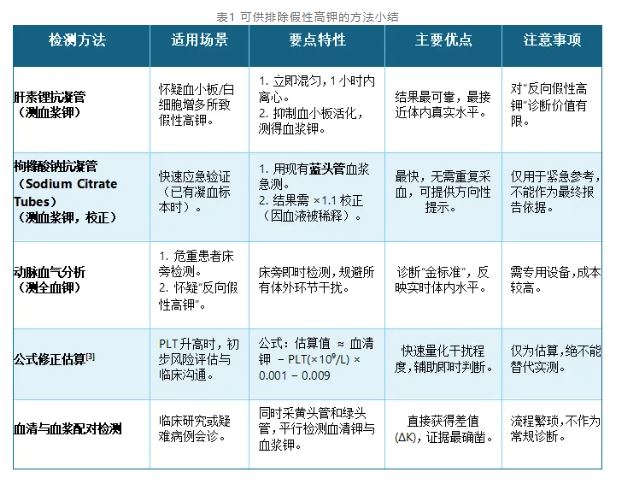
使用建议总结:①常规首选:采集肝素锂抗凝管复查血浆钾。②紧急验证:利用现有枸橼酸钠 抗凝管血浆检测并校正,作为快速参考。③金标准:危重或复杂病例推荐动脉血气分析。
抗凝管血浆检测并校正,作为快速参考。③金标准:危重或复杂病例推荐动脉血气分析。
案例小结
本案例呈现了一例由外周血全细胞增多导致的假性高钾血症。患者血清钾达6.20 mmol/L的危急值,而肝素锂抗凝血浆钾仅为4.75 mmol/L,两者间的巨大差异,揭示了体外凝血过程中血细胞协同释钾的关键机制:
血小板活化是钾释放的主要来源;白细胞增多加速ATP耗竭,致使钠钾泵功能衰竭,促使胞内钾外流;而红细胞增多则构成了巨大的“钾库”,并在高粘状态下更易受离心等机械因素影响而释放钾离子。正是这些因素的体外叠加,共同造成了血钾假性升高的“P图”效应。
面对不符合临床表象的高钾结果,检验人应当具备“先辨真假”的系统性思维。当高钾伴随血细胞显著增多时,应主动同临床沟通,采取合理方式去伪求真,以规避体外干扰。这不仅是检验科对检验质量的不懈追求,更是架设在检验与临床之间的重要桥梁——通过精准的实验室数据,协助临床避免误诊和不必要干预,共同筑牢患者安全防线。
专业审核:张海东(北京市普仁医院)
参考文献
[1]刘晓叶,胡蕊,李刚 ,等.假性高血钾症的识别与避免[J].中华高血压
,等.假性高血钾症的识别与避免[J].中华高血压 杂志,2018,26(08):784-789.DOI:10.16439/j.cnki.1673-7245.2018.08.026.
杂志,2018,26(08):784-789.DOI:10.16439/j.cnki.1673-7245.2018.08.026.
[2]李进 ,袁朋超,邹刊,等.血小板与白细胞增多致假性高钾血症1例[J].罕少疾病杂志,2025,32(07):22-23.
,袁朋超,邹刊,等.血小板与白细胞增多致假性高钾血症1例[J].罕少疾病杂志,2025,32(07):22-23.
[3]瞿晓媛,徐益恒 ,邰文琳,等.血小板增多
,邰文琳,等.血小板增多 导致血清假性高钾的修正[J].昆明医科大学学报,2020,41(05):125-129.
导致血清假性高钾的修正[J].昆明医科大学学报,2020,41(05):125-129.
来源:检验医学网
