
图解乳“献”|第131期:ESR1激活突变通过抑制细胞因子分泌,促成免疫抑制型乳腺肿瘤微环境
本期配图来自2026年3月9日发表在JCI Insight(IF 6.1 )上的文章《Activating mutations in ESR1 contribute to an immunosuppressive breast tumor microenvironment by dampening cytokine secretion》[1]
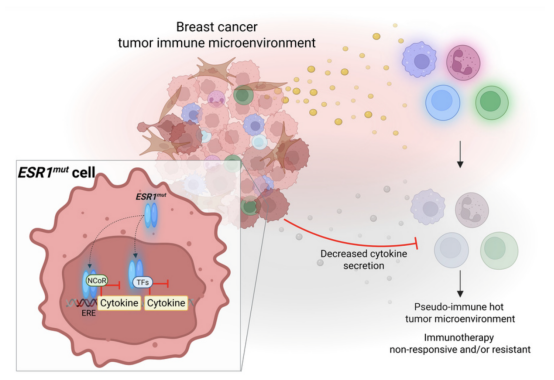
图1. ESR1突变致使乳腺肿瘤免疫抑制机制示意图[1]
本图介绍了ESR1激活突变导致乳腺肿瘤免疫抑制的分子机制。突变型ESR1导致受体配体非依赖性活化,一方面直接下调免疫调节基因转录,另一方面上调肿瘤上皮细胞STAT5信号,活化的STAT5进一步结合并抑制IL-17a及IL-1b表达,促使浸润T细胞与巨噬细胞功能麻痹,形成免疫细胞数量正常但活性受抑的微环境。该机制的阐明为改善ER阳性乳腺癌 免疫治疗疗效提供了新的干预靶点与理论依据。
免疫治疗疗效提供了新的干预靶点与理论依据。
突变型ESR1获得配体非依赖性转录活性
ESR1基因发生Y541S或D542G激活突变后,其编码的雌激素 受体配体结合域构象发生改变,使受体在无雌激素刺激下仍维持持续活化状态。相较于野生型ESR1,突变型受体在染色质招募及转录辅调节因子募集方面呈现差异性特征,在维持细胞周期相关基因上调的同时,对一系列免疫调节基因启动负性调控。
受体配体结合域构象发生改变,使受体在无雌激素刺激下仍维持持续活化状态。相较于野生型ESR1,突变型受体在染色质招募及转录辅调节因子募集方面呈现差异性特征,在维持细胞周期相关基因上调的同时,对一系列免疫调节基因启动负性调控。
肿瘤上皮细胞内STAT5信号通路激活
在突变型ESR1的驱动下,肿瘤上皮细胞中STAT5总蛋白表达水平及其磷酸化激活水平均显著上调,而STAT3信号通路未见明显变化。上调的STAT5作为关键转录因子,与突变型ESR1形成协同调控网络,共同参与下游免疫相关基因的表达调控。
STAT5介导细胞因子基因转录抑制
活化的STAT5可直接结合至IL-17a及IL-1b等细胞因子基因启动子区域,通过竞争性占据STAT3结合位点,拮抗STAT3介导的转录激活,抑制细胞因子转录,促使肿瘤上皮细胞来源IL-17a及IL-1β转录水平显著下调。
上皮源细胞因子匮乏诱导免疫抑制发生
IL-17a及IL-1β等关键免疫调节细胞因子的减少,直接削弱了浸润免疫细胞功能激活能力。尽管CD45+免疫细胞、CD3+T细胞及F4/80+巨噬细胞的总体浸润数量未发生改变,但T细胞IFN-γ产生能力与巨噬细胞MHC II抗原呈递功能均显著受损,最终形成免疫细胞浸润但功能受抑的免疫抑制性肿瘤微环境。
背景补充
ESR1激活突变是ER阳性乳腺癌内分泌治疗耐药的关键机制,约30%的晚期患者携带此类突变。临床上,这类患者对免疫治疗响应不佳,但突变本身如何主动重塑肿瘤免疫微环境尚不明确。本研究通过构建携带临床常见ESR1突变的转基因小鼠模型,系统揭示了突变型ESR1调控肿瘤细胞因子分泌、进而影响免疫细胞功能的分子机制。
参考文献:
Gu Y, Zuo D, Hu QX, et al. Activating mutations in ESR1 contribute to an immunosuppressive breast tumor microenvironment by dampening cytokine secretion. JCI Insight. 2026;11(5):e199927. Published 2026 Mar 9. doi:10.1172/jci.insight.199927

往期推荐
编辑:Ocean
审校:KIKI
排版:KIKI
执行:KIKI
医脉通是专业的在线医生平台,“感知世界医学脉搏 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
